О подходе к построению модели дистальных сосудов пригодной для оценки артериального давления
Аннотация
В статье рассмотрен подход к созданию модели на основе нейросети для использования в фотоплетизмографах. С использованием данной модели возможна разработка метода измерения артериального давления в дистальном отделе сосудов. Подобный подход позволяет обеспечить комфортный съем диагностических параметров при необходимости проведения длительного обследования. Данные методы применимы для анализа состояния человека-оператора, и в частности, водителя при предсменном контроле, для скриннинговых обследований.
Ключевые слова: фотоплетизмограмма, сердечно-сосудистая система, нейросети, моделирование
05.13.18 - Математическое моделирование, численные методы и комплексы программ
В настоящее время разработано достаточное количество неинвазивных методов для оценки состояния сердечно-сосудистой системы: они безопасны для здоровья пациента, точны и дешевы в применении.
Одним из достаточно комфортных методов является фотоплезмография [1]. В основном конструктивно фотоплетизмографические датчики представляют собой игольчатый инфракрасный излучатель (ИК), который посылает в палец руки световой поток, рассеивающийся на дистальных артериях. Зачастую используют две длины волны λ1 = 660 нм – красный свет и λ2 = 940 нм – инфракрасный свет, т.е. выбраны те длины волн, для которых разность между коэффициентами поглощения оксигемоглобина и гемоглобина максимальна и различна по знаку, а влияние карбоксигемоглобина и метгемоглобина минимально [2].
В комплексном обследовании состояния человека измерение систолического и диастолического давления является одним из важных параметров. Достоверное измерение АД и правильная постановка диагноза – один из главных факторов, вносящих свой вклад в лечение артериальной гипертензии – одного из самых массовых заболеваний нашего времени.
Традиционно принятый рутинный осциллометрический метод измерения АД в плечевой артерии при обследовании пациента является не очень удобным и локализованным во времени методом [3]. При обследовании состояния человека-оператора, предсменном контроле водителей, летчиков, в критической медицине и т.п., комфортное измерение давления играет важную роль, т.к. стандартное измерение на основе тонов Короткова может быть невозможно.
Давление связано с кровотоком и скоростью прохождения гидродинамических волн внутри сосудов [4]. Но давление в сосудах не имеет постоянного значения и изменяется во времени. Время распространения пульсовой волны определяется временем от начала импульса возбуждения в сердце до появления переднего фронта волны в сосуде. Это время зависит от объема левого желудочка, от силы сокращения и частота сокращений желудочка. Также время распространения пульсовой волны по сосудистому руслу зависит от длины сосуда и среднего значения давления.
Основной целью разработки модели является определение значений систолического и диастолического давления. Точно измерить эти значения возможно только с помощью инвазивных методов, и измерение в любом случае будет с ошибкой. Даже если измерять очень точно, вряд ли значения совпадут с измерениями по принятой методике по тонам Короткова. Точность осциллометрических приборов имеет свои ограничения. Погрешность измерения давления методом Короткова соответствует:
• ± 5мм рт.ст. для среднего давления;
• ± 8мм рт.ст. для систолического и диастолического давления [3].
В настоящее время широкое распространение получило использование искусственных нейронных сетей для построения математических моделей сложных нелинейных процессов, распознавания образов и прогнозирования сигналов. Нейронная сеть – это набор нейронов, каждый из которых представляет собой модель биологического нейрона. В настоящее время широко используются математические модели нейронных сетей [5]. Если, задаться целью, получить значения систолического и диастолического давления, совпадающие со значениями, измеренными по тонам Короткова, то на модель созданную методом нейронных сетей накладываются следующие требования: модель должна принимать на вход небольшое количество прямо измеренных параметров, максимально влияющих на два требуемых выходных параметра - систолическое и диастолическое давление. И обработка и верификации модели в этом случае должна идти по пути отбора входных параметров, оценки трансформированной погрешности при устранения артефактов, которые могут возникнуть в процессе измерения данными методами, т.к. во время измерения положение руки может быть различным (рука согнута и лежит, поднята, опущена).
Достаточно точно можно измерить время начала R-зубца, приблизительно длину сосудистого русла и мгновенные значения откликов фотоплетизмограммы.
Для обучения нейросети воспользуемся методом тонов Короткова. Тогда, входные параметры можно разделить на две группы – дискретные и континуальные. К дискретным параметрам относятся точечные оценки ЧСС и длина сосудов, измеренные с определенной точностью, и континуальные параметры – отклики ФПГ за один сердечный цикл. При частоте дискретизации fдиск.=200-250 Гц, получится 200-300 точек. Чувствительность выходных параметров относительно изменения входных точек будет различной. Анализируя ФПГ можно получить дополнительные параметры, характеризующие гидродинамическую картину в дистальном отделе сосуда. Измеряя время прохождения импульса ФПГ можно получить время распространения пульсовой волны, зафиксировать длительное повышение давления в дистальном отделе, время появления обратной волны. В общем случае у всех людей ФПГ имеет два участка – анакрота и катакрота. Поскольку данная методика не ориентирована на выявление тонких изменений в исследуемом сосуде, а нацелена на получение двух интегральных параметров, то желательно иметь простые модели этих двух участков ФПГ. Наиболее простым решением является применение кубического сплайна для моделирования этих участков. В отличие от ЭКГ, где функция на месте R-зубца имеет разрыв второй производной, а часто и первой производной, вершина ФПГ разрывов не имеет, в силу физических причин, поэтому применение сплайна здесь оправдано. Использование такой модели сразу дает сокращение входных точек нейросети с 300 параметров до 8. Используя 8 параметров и зная время распространения пульсовой волны и частоту пульса, мы получаем модель с десятью входными параметрами и двумя выходными параметрами. Исследование такой модели можно проводить средствами, имеющимися в пакетах Matlab . Основной смысл исследования заключается для определения применимости ФПГ для измерения давления в сосудах.
Записанная ФПГ считывается из файла с помощью функции:
FID=fopen('c:\users\name\documents\3.fpg');
[A,count]=fscanf(FID,'%f');
После координаты вершины определяются следующим оператором:
[CM,Imax]=max(A);
Выделив анакроту и участок катакроты, соответствующий систолической волне, можно построить аппроксимирующие их полиномы методом наименьших квадратов:
X=(5:22)';
B=A(5:22);
p = polyfit(X, B, 3);
X3=(23:40)';
B1=A(23:40);
p1 = polyfit(X3, B1, 4);
Полученные значения коэффициентов полинома p:
-0,4394 17,1511 -149,1347 373,1072
Полученные значения коэффициентов полинома p1:
0,1180 -11,1226 318,0880 -2142,8564
Далее можно восстановить анакроту и катакроту используя следующие функции:
ff = polyval(p, X);
ff1= polyval(p1, X3);
plot(X3, ff1, '-r', X, ff, '-g', X1,C, 'ob');
Как видно на рисунке 1, полиномы достаточно хорошо отражают ход систолической волны ФПГ.
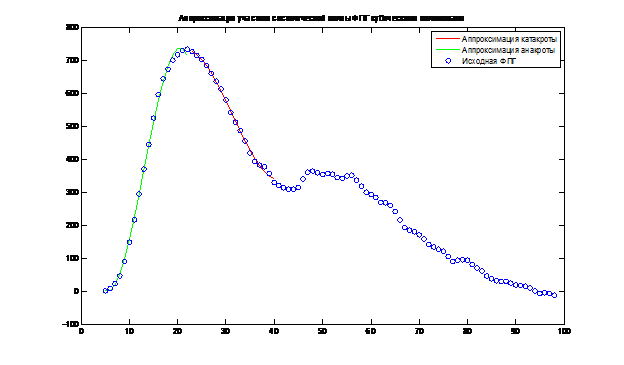
Рисунок 1 – Аппроксимация участков систолической волны ФПГ кубическим полиномом
Построение нейронной сети наиболее удобно сделать с использованием GUI NNTool из пакета Matlab. При этом, например, входные вектора можно импортировать прямо из рабочей области Matlab с помощью клавиши Import, как показано на рисунке 2.
Рисунок 2 - Импорт входных векторов при построении нейросети
Аналогично на рисунке 3 показано задание выходных параметров нейросети.
Рисунок 3 - Импорт выходных векторов при построении нейросети
После задания векторов синтез нейросети осуществляется с помощью специального диалогового окна. Например, при задании 1 скрытого слоя с 10 нейронами на входе и 1 нейрона в выходном слое для генерирования систолического давления синтезируется нейросеть, показанная на рисунке 4.
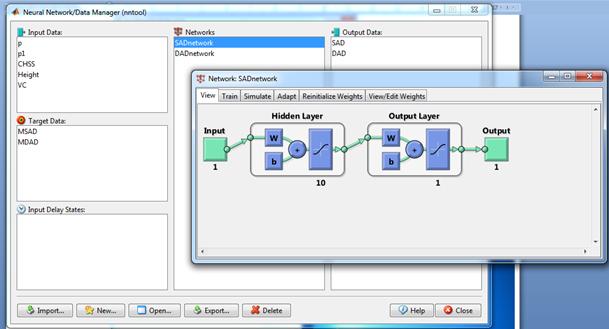
Рисунок 4.-Структура нейросети для оценки систолического давления
Дальнейшая работа с построенной нейросетью, обучение и верификация, осуществляется по известным методикам [6].
Предлагаемую модель предполагается исследовать на применимость для измерения систолического и диастолического давления с помощью фотоплетизмографа. Применение такого подхода позволит измерять давление достаточно комфортно, что удобно при проведении длительного мониторирования, исследований состояния человека-оператора и медицине катастроф.
Результаты исследований изложенные в данной статье получены при финансовой поддержке Минобрнауки РФ в рамках реализации проекта "Создание высокотехнологичного производства по изготовлению информационно-телекоммуникационных комплексов спутниковой навигации ГЛОНАСС/GPS/Galileo" по постановлению правительства №218 от 09.04.2010 г.
Список литературы:
- Семенистая Е.С. Применение двухчастотной оксиметрии для оценки состояния человека-оператора. Известия Южного федерального университета. Технические науки. 2004. Т. 41. № 6. С. 58-61.
- Семенистая Е.С. Диагностические показатели контура пульсовой кривой Известия Южного федерального университета. Технические науки. 2008. Т. 79. № 2. С. 111-116.
- Синютин С.А. Оценка состояния сердечно-сосудистой системы на базе экг и оксигемометрии Известия Южного федерального университета. Технические науки. 2010. Т. 106. № 5. С. 80-84
- Галкин М., Змиевской Г., Ларюшин А., Новиков В. Кардиодиагностика на основе анализа фотоплетизмограмм с помощью двухканального плетизмографа // М:Техносфера - Фотоника. 2008. - № 3 - С. 30-35.
- Bayir, R. Kohonen Network based fault diagnosis and condition monitoring of serial wound starter motors [Text] / R. Bayir, O. F. Bay: IJSIT Lecture Note of International Conferense on Intelligent Knowledge Systems. – 2004. – Vol. 1, - № 1.
- http://paukoff.fromru.com/neuro/wneuro/index.html Прогнозирование с помощью искусственных нейронных сетей [Электронный ресурс] (Дата обращения 15.11.2012г.)